Anticorps monoclonaux
Cette page dédiée aux anticorps monoclonaux dans le traitement des formes symptomatiques légères à modérées de COVID-19 chez les adultes à risque d’évoluer vers une forme grave, comprend des informations utiles sur les modalités de prescription et d’administration, de prise en charge, de surveillance et d’approvisionnement de ceux-ci.
Retrouvez ci-après les informations :
| Anticorps monoclonaux disponibles | |||
| Bamlanivimab | Modalités de prescription et d’administration | Cliquez ici | |
| Fiche pratique (OMEDIT Pays de la Loire) | Cliquez ici | ||
| Casirivimab/ Imdevimab | Modalités de prescription et d’administration | Cliquez ici | |
| Fiche pratique (OMEDIT Pays de la Loire) | Cliquez ici | ||
| Bamlanivimab/Etesivimab | Modalités de prescription et d’administration | Cliquez ici | |
| Fiche pratique (OMEDIT Pays de la Loire) | Cliquez ici | ||
| Prise en charge des patients éligibles | Cliquez ici | ||
| Liste des établissements proposant un traitement par anticorps monoclonaux | Cliquez ici | ||
| Surveillance | Cliquez ici | ||
| Modalités d’approvisionnement des établissements de santé | Cliquez ici | ||
Anticorps monoclonaux disponibles
>> Bamlanivimab :
- Modalités de prescription et d’administration :
- ATU de cohorte obtenue le 22 février 2021, dans l’indication « des formes symptomatiques légères à modérées de COVID-19 chez les adultes à risque d’évoluer vers une forme grave »
- RCP : cliquez ici
- Documents de référence pour l’ATU de cohorte (ANSM) : cliquez ici
- Critères d’inclusion/d’exclusion : cliquez ici
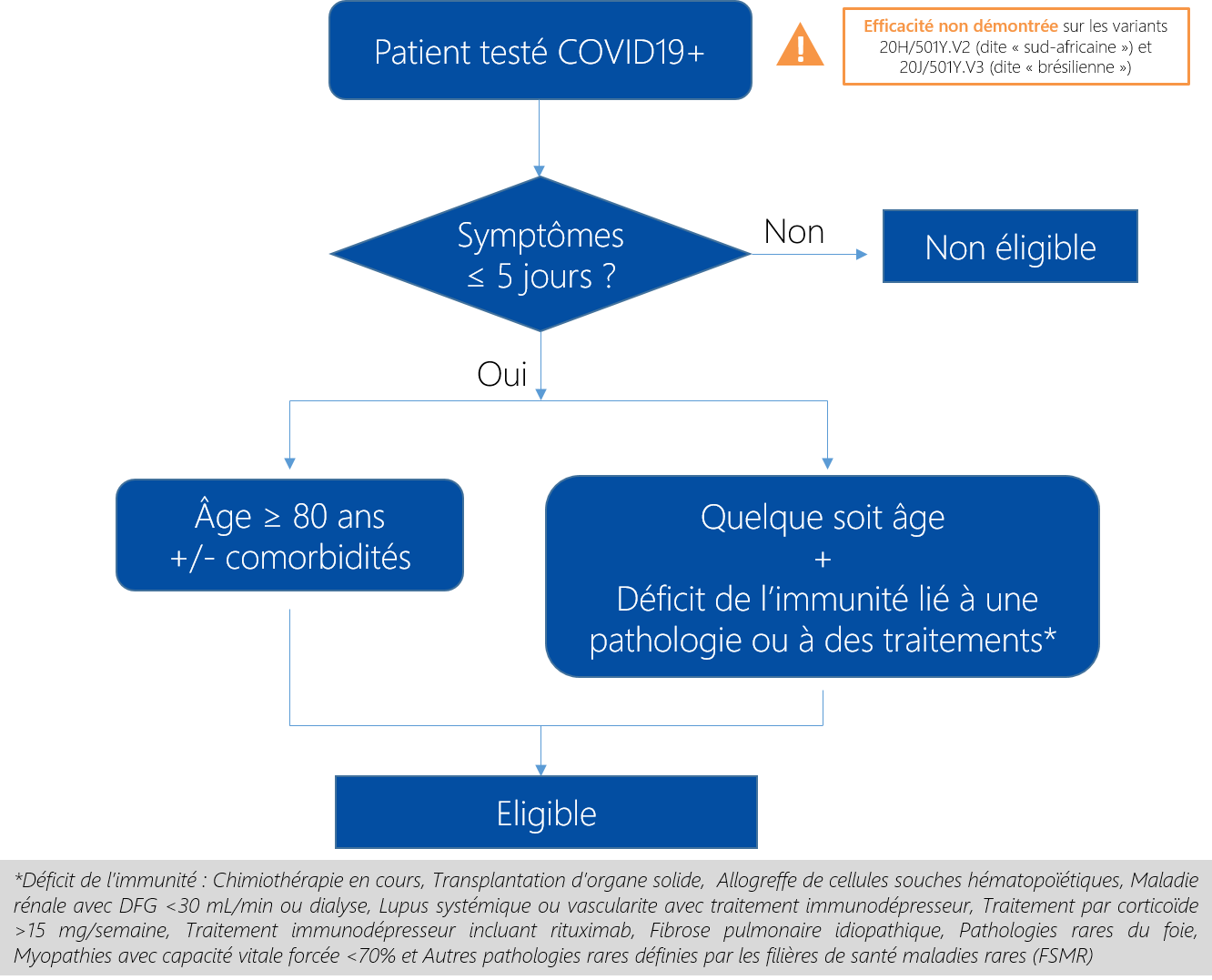
- Outils disponibles :
- Retrouvez notre fiche pratique :

- Prise en charge des patients éligibles :
- Infographie « Patients » – Critères d’éligibilité et modalités de prise en charge (Ministère des Solidarités et de la Santé) /
Cliquez ici - Infographie « Professionnels de santé » – Critères d’éligibilité et modalités de prise en charge (Ministère des Solidarités et de la Santé) : Cliquez ici
- Infographie « Patients » – Critères d’éligibilité et modalités de prise en charge (Ministère des Solidarités et de la Santé) /
>> Casirivimab/Imdevimab :
- Modalités de prescription et d’administration :
- ATU de cohorte obtenue le 17 mars 2021, dans l’indication « des formes symptomatiques légères à modérées de COVID-19 chez les adultes à risque d’évoluer vers une forme grave »
- RCP : cliquez ici
- Documents de référence pour l’ATU de cohorte (ANSM) : cliquez ici
- Critères d’inclusion/d’exclusion : cliquez ici
>> Bamlanivimab/Etesivimab :
- Modalités de prescription et d’administration :
- ATU de cohorte obtenue le 16 mars 2021, dans l’indication « des formes symptomatiques légères à modérées de COVID-19 chez les adultes à risque d’évoluer vers une forme grave »
- RCP : cliquez ici
- Documents de référence pour l’ATU de cohorte (ANSM) : cliquez ici
- Critères d’inclusion/d’exclusion : cliquez ici
Surveillance
Concernant les informations sur la surveillance du traitement lors de l’administration, se référer au RCP ou au protocole d’utilisation thérapeutique (PUT) de chaque spécialité pharmaceutique.
Pour rappel, tout effet indésirable suspecté doit être déclaré sans délai via :
- Système national de déclaration sur le site internet : cliquez ici
- Centre Régional de Pharmacovigilance : CRPV Nantes ou CRPV Angers
Modalités d’approvisionnement des établissements de santé
- Mise à disposition des établissements de santé :
L’Etat met à disposition des établissements de santé les spécialités pharmaceutiques : BAMLANIVIMAB 700 mg/20 mL
CASIRIVIMAB et IMDEVIMAB 120 mg/mL ROCHE ;
BAMLANIVIMAB et ETESEVIMAB 700 mg/20 mL LILLY
Les livraisons sont réparties dans les établissements de santé.
- Suivi des stocks sur la plateforme e-Dispostock :
Il est demandé aux établissements de santé de renseigner trois fois par semaine le nombre de flacons en stock et dès toute réception.
Un suivi régional (ARS) et national sera effectué pour gérer d’éventuelles tensions et prioriser la livraison de doses.
Retrouvez notre dossier COVID-19 :




